含有硅手性的有机硅化物因其独特的结构和性质,在有机合成、功能材料及生物医药等领域展现出特有的价值和应用前景。因此,如何高效构建硅中心手性有机硅化物逐渐成为了有机化学家们的研究热点。近日,山东大学前沿交叉科学青岛研究院分子科学与工程研究院李兴伟教授团队实现了铑催化简单易得苄醇、亚胺与二级硅烷的不对称[4 1]环化反应,高效地合成了含有硅手性的杂环化合物。相关成果以“rhodium-catalyzed enantioselective formal [4 1] cyclization of benzyl alcohols and benzaldimines: facile access to silicon-stereogenic heterocycles”为题,发表在国际著名期刊angew. chem. int. ed.上。博士后申兵学为本文第一作者,李兴伟教授、于松杰教授和天津大学黄跟平教授为通讯作者,山东大学为该论文的第一完成单位。
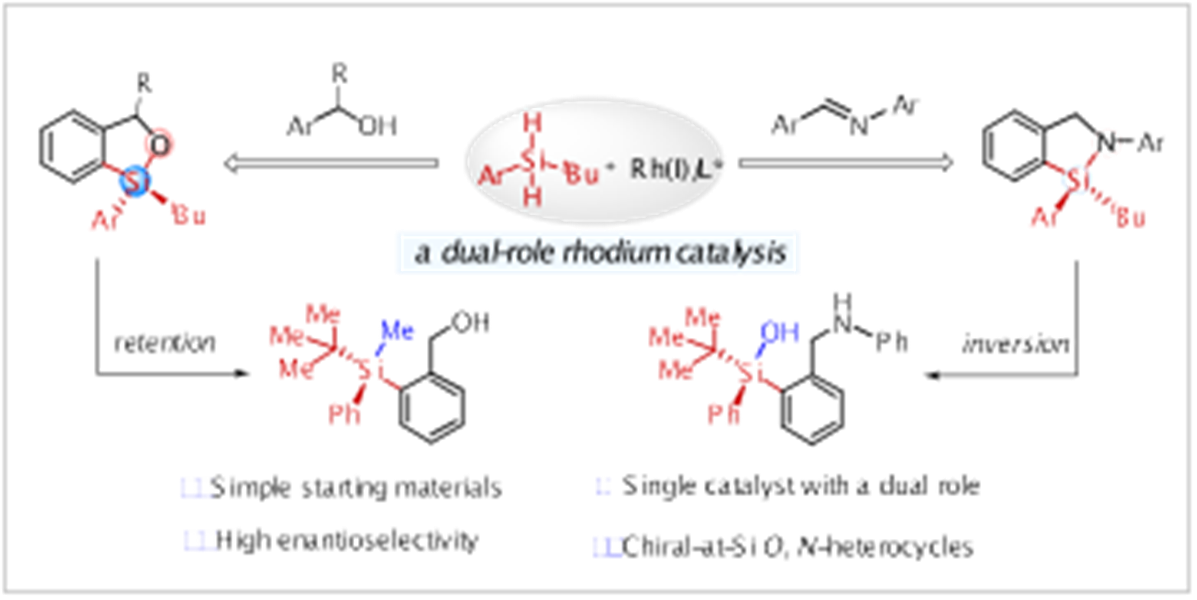
图一 铑催化构筑硅手性杂环化合物

图二 部分苄醇反应产物实例
当以苄醇为底物,通过铑催化苄醇与二氢硅烷的脱氢偶联/串联c-h活化硅化反应,首次实现铑催化分子间c-h硅化反应构筑含硅立体中心环状化合物。该反应对各类取代基都有良好的耐受性,能够以较高收率、优异的对映选择性得到目标产物(图二)。此外,本文还研究了铑催化亚胺与二氢硅烷的不对称[4 1]环化反应,其中由于产物结构中包含si-n键,不利于产物柱色谱分离,该反应目标产物用无机碱后处理,得到构型翻转的开环产物,对映选择性未衰减,该反应对带有各类取代基的亚胺底物也具有良好的耐受性(图三)。
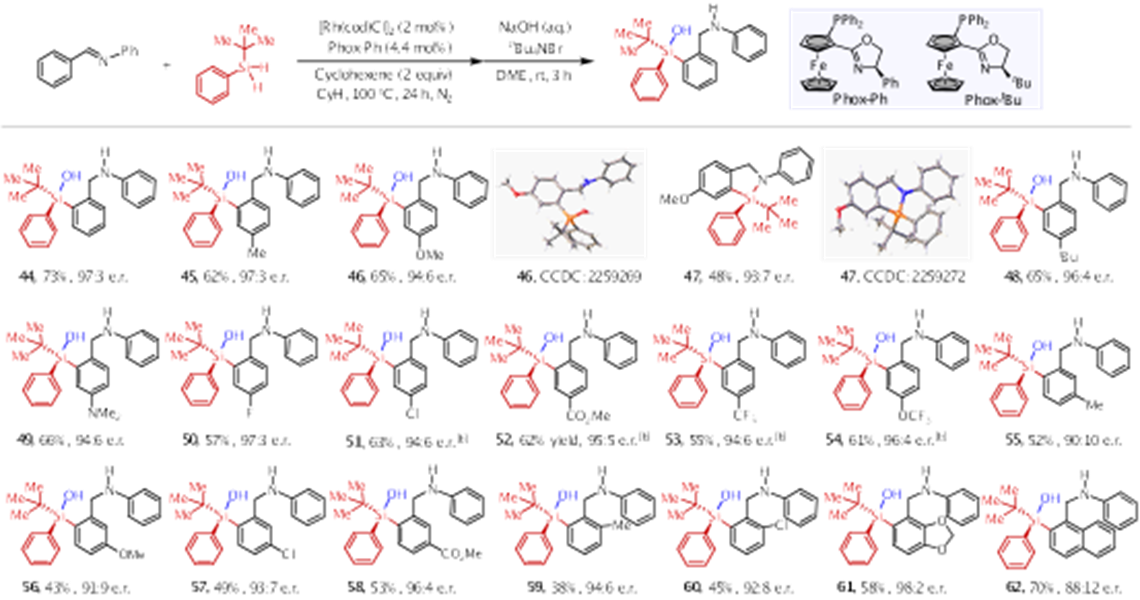
图三 亚胺反应部分产物实例
天津大学黄跟平教授对苄醇羟基硅化过程进行理论计算,发现 (r)-ts3、(s)-ts3硅氧键还原消除过渡态能量差值为3.1kcal/mol,该差值可以很好吻合实验过程中得到优秀的立体选择性的结果,并说明硅氧键还原消除是整个过程中的立体决定步骤(图四)。
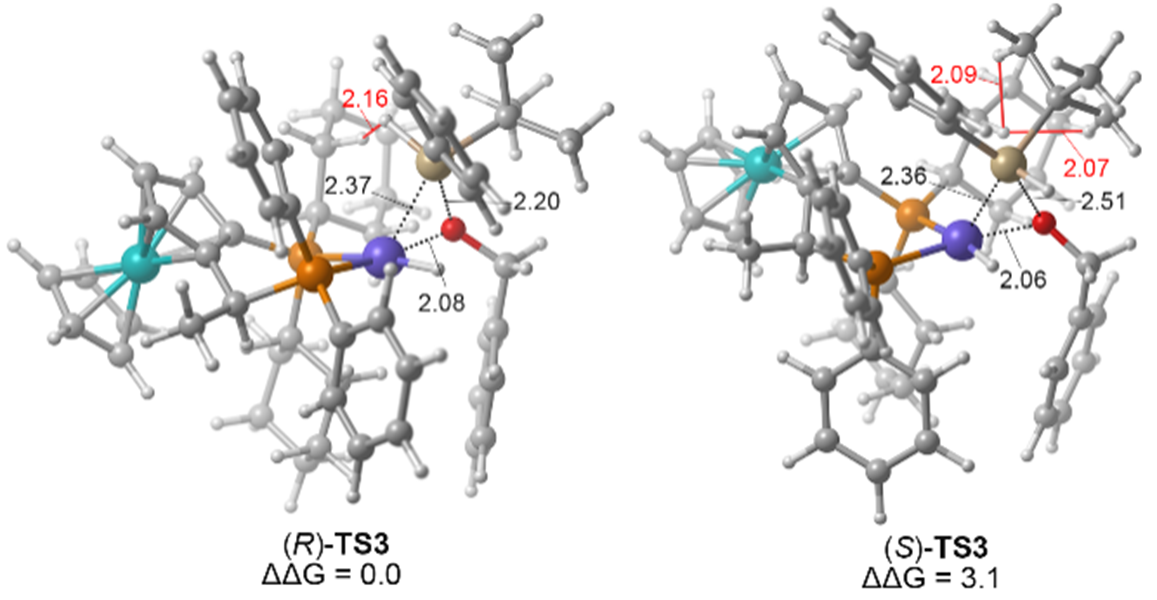
图四 立体决定步骤研究(计算化学)
综上所述,山东大学前沿交叉科学青岛研究院分子科学与工程研究院李兴伟教授团队实现了首例单一金属催化分子间c-h键硅化构筑硅中心手性杂环化合物的反应。该反应适用范围广,具有较高的合成应用价值。上述工作得到山东大学双一流建设经费资助。
论文链接:


