氮氮轴向手性联芳基化合物是一类研究较少的阻转异构体。近日,前沿交叉科学青岛研究院分子科学与工程研究院李兴伟教授团队与合作者通过合理的底物设计,进行了含有氮氮和碳氮/碳碳双轴的手性联芳基化合物的构建,该反应具有优异的对映选择性和非对映选择性(图1)。相关成果以“rhodium-catalyzed enantioselective anddiastereodivergentaccess to diaxiallychiral heterocycles”为题,发表在国际知名期刊nature communitions(中科院一区,top,if=16.6)上。前沿交叉科学青岛研究院2019级博士生王义收为第一作者,李兴伟教授、黄根平教授(天津大学)和王芬教授(陕西师范大学)为通讯作者,山东大学为第一完成单位。
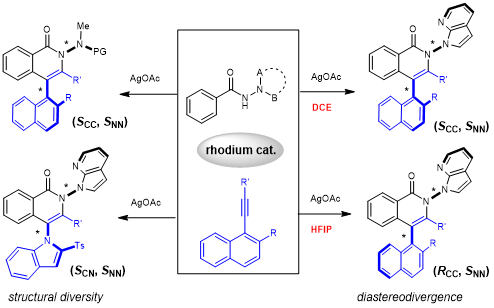
图1 氮氮和碳氮/碳碳双轴手性联芳基化合物的构建
氮氮轴向手性较为罕见,这要求有机合成工作者们在开发新的合成方法上进行探索;在本研究中,李兴伟教授团队将氮氮轴手性和非对映发散结合起来,同时报告了三类具有优异的对映选择性和非对映选择性的含有氮氮和碳氮/碳轴双轴的手性联芳基化合物。其中的亮点是,在一定反应条件的控制下,罕见的非对映发散在大范围的酰胺和1-炔基萘的不对称耦合中被实现(图2)。黄根平教授团队的计算研究为非对映发散的形成提供了较为深入的机理解释。
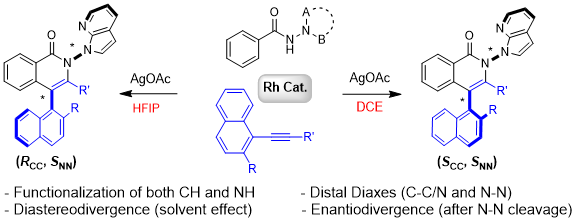
图2 反应条件控制的双轴立体发散
团队之前对1-炔基萘和芳烃的铑催化偶联进行过研究(angew. chem. int.ed.2020, 59, 13288–13294. &angew. chem. int. ed.2021, 60, 16628–16633.),即使使用固定类别的手性环戊二烯基铑(iii)催化剂,也可得到两种不同的手性轴构型(图3):炔插入的立体化学似乎与溶剂的性质有关;质子性溶剂和非质子性溶剂的作用趋势可能不同。在非质子性溶剂中,lewis酸添加剂ag(i)或zn(ii)可能参与连接导向基团和大位阻炔的2-or基团,对大位阻炔的插入方向进行了明确定位。
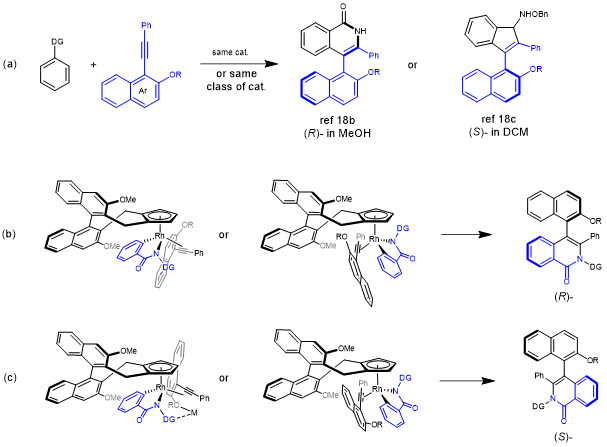
图3 大位阻炔对映选择性插入中可能的立体发散和手性诱导模型
经过对酰胺底物的广泛探索,作者最终实现了7-氮杂吲哚苯酰胺与1-炔基萘偶联的非对映发散。正如预期的结果,当dce作为溶剂时,可以在(scc,snn)选择性下合成环状产物(条件c)。相反,当强氢键极性溶剂hfip(条件d)被使用时,可以得到非对映异构体(rcc,snn)。然后作者详细探讨了非对映异构发散的范围,该反应对各种取代基团适用性良好(图4)。
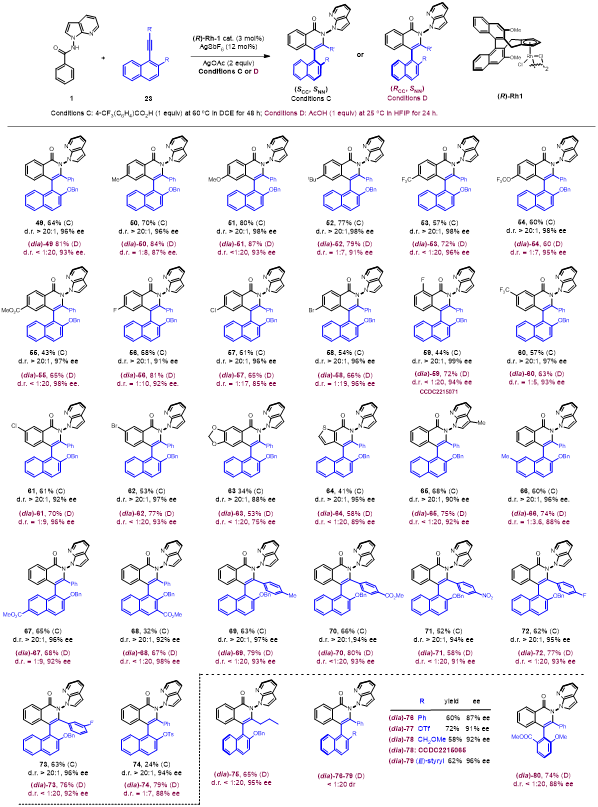
图4 [4 2]环化反应的非对映发散适用范围
该产物中的氮氮键可以在温和的条件下发生断裂。作者使用smi2处理双轴产物使导向基快速去除,得到了含有单个碳碳手性轴的产物。通过这个简单的操作,两种非对映体产物被转化为相应的对映异构体(图5)。
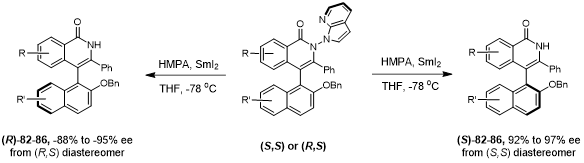
图5 氮氮键的裂解实现非对映异构体的对映发散
综上所述,李兴伟教授团队报道了一种铑催化对映选择性和非对映选择性良好的构建双轴手性联芳基化合物的方法。该反应条件温和,适用范围广,具有潜在的合成应用价值。上述工作的得到山东大学双一流学科建设经费的资助。
原文链接:


